脊椎動物の生物時計においては、時計遺伝子の中でも負の制御因子と呼ばれるPer・Cry遺伝子のE-box依存的転写を正の制御因子であるCLOCKとBMAL1のヘテロ二量体が(昼に)活性化し、転写・翻訳されたPER/CRY複合体がCLOCK-BMAL1による転写活性化を(夜に)抑制する。このようなE-boxに依存した転写活性化のフィードバックループが、約24時間で活性化と抑制のサイクルを繰り返して分子時計を形成している(図1)。この分子時計の謎は次の4点に集約される:(i) いかにして24時間という長い周期を形成できるのか? (ii) なぜ何サイクルにもわたって安定に発振できるのか? (iii) その位相を制御する(光などの)シグナルはどのように入力するのか? (iv) 分子時計によって形成された分子発振がいかにして生理機能のリズムに出力するか? これらの謎を秘めた概日時計システムの理解に向けて我々は、一群の時計遺伝子の転写調節ネットワーク(図1)が時計蛋白質の翻訳後修飾(リン酸化など)によって制御されるメカニズムの解明に取り組んでいる。
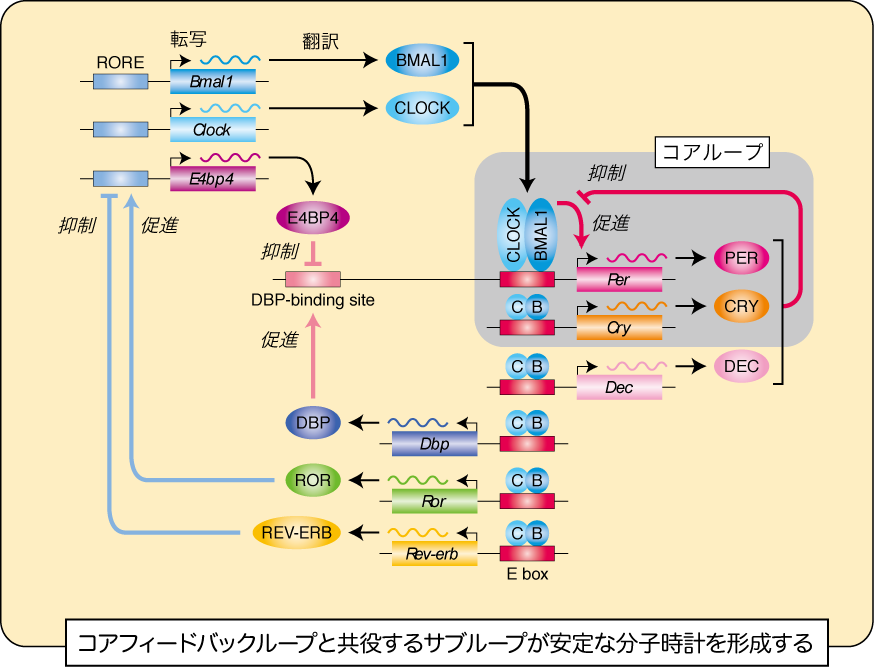 図1.時計遺伝子の転写と翻訳に基づく24時間周期の分子時計の振動メカニズム
[広田毅・深田吉孝 (2004) 実験医学, Vol.24, No. 4, pp. 452-459より改変]
図1.時計遺伝子の転写と翻訳に基づく24時間周期の分子時計の振動メカニズム
[広田毅・深田吉孝 (2004) 実験医学, Vol.24, No. 4, pp. 452-459より改変]これまでに我々は、Per遺伝子の転写を抑制する時計蛋白質CRY2とE4BP4がそれぞれGSK-3βとCKIεによってリン酸化され、このリン酸化がこれら時計蛋白質の機能を調節すると共に、急速な蛋白質分解に導くことを見出した (J. Biol. Chem. 2005; Curr. Biol. 2004)。CRY2もE4BP4も、それぞれ異なる蛋白質キナーゼ(未知のプライミングキナーゼ)によって第一段階目のリン酸化を受けた後、逐次的に起こる2段階目のリン酸化が分解シグナルとなって26Sプロテアソームによる分解に導かれる。現在、これらのキナーゼの同定とその活性を制御するメカニズムを調べると共に、分解へと導くリン酸化配列を認識するユビキチンリガーゼの同定をめざしている。一方、蛋白質量が一定に見える正の制御因子CLOCKが、やはりリズミックにリン酸化されて時刻特異的に26Sプロテアソームによって分解されていることを見出した。このように24時間という長い周期を安定に維持する仕組みとして、時計蛋白質の機能制御とタイムリーな蛋白質分解は、分子時計において極めて重要な位置を占める。当研究グループでは行動リズムの周期に異常を示す数多くの遺伝子改変マウスを維持し、これらマウスのin vivoデータ、行動リズムの測定、および分子レベルの解析から統合的に生体での時計発振の実態に迫ろうとしている。
概日時計は一方で、多様な刺激(位相制御因子)により時刻特異的に位相シフトするという特性を持つ。我々はニワトリ松果体を用いた実験から、Perの転写抑制を導く時計制御遺伝子E4bp4が夜更かしの光刺激で誘導されることを見出し、Per遺伝子上流のDBP-binding siteを介した時刻特異的な位相後退の分子メカニズムを示した (PNAS 2001)。その後、光誘導遺伝子の網羅的な解析から「夜更し」や「早起き」の光シグナルで誘導される一群の遺伝子を同定し、その機能解析から光位相制御の解明を目指している。
動物の生物時計は中枢のみならず末梢の多くの細胞に存在し、これらは中枢時計を頂点とするヒエラルキーの中で同調し、動物個体の大きなリズムを形作っている。中枢時計による末梢時計の制御には、交感神経を介した神経性支配と共に、血流などを介した液性因子による制御が知られている。光刺激は直接的には中枢時計の位相を制御するが、光と並ぶ重要な位相制御因子である食餌は、肝臓などの末梢時計の位相を制御する。我々は末梢時計のモデル系として株化培養細胞を用い、食餌の主要代謝産物であるグルコースが細胞時計をリセットすることを見出した。光刺激による位相シフトにはPer2遺伝子の一過的な転写誘導が必須であるが、グルコース刺激による位相シフトではPer2のmRNAレベルはむしろ低下する。Per2の誘導を伴わない新規の位相シフト機構を探るため、グルコース刺激で誘導される遺伝子を網羅的に調べ、刺激後すみやかに誘導されるTieg1を見出した (J. Biol. Chem. 2002)。この遺伝子がコードする転写抑制因子TIEG1が、(時計)遺伝子の転写をどのように制御し、どのように位相シフトを引き起こすのか、現在その分子機構を調べている。
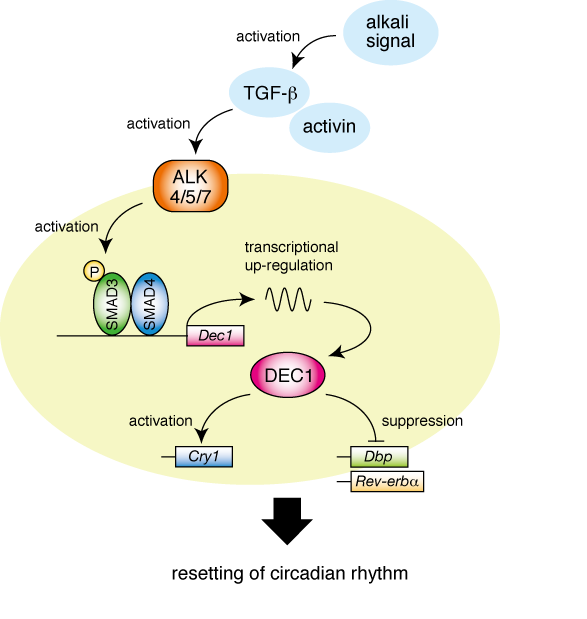
この研究の過程で我々は、TGF-βあるいはactivinというタンパク質因子が非常に強い時計リセット活性を持つことを見出した (Nat. Cell Biol. 2008)。TGF-βは細胞の増殖抑制因子として知られ、そのシグナル異常が発癌を起こすことや、その他、多様な生命現象に関与する因子として知られていたが、TGF-βやactivinが全身に広く分布して生物時計を制御することは予想もされていなかった。これらの刺激によって時計位相がリセットされる時に時計遺伝子の発現を解析したところ、bHLH型転写因子をコードするDec1遺伝子がすばやく一過的に発現誘導されることがわかった。Dec1は2002年、北大(医)本間教授と広島大(医)加藤教授らのグループによって時計制御因子としての重要性が示された (Honma et al., Nature 2002)。しかしその後、Dec1欠損マウスの行動がほぼ正常なサーカディアンリズムを示すことが判明し、時計システムにおける生理的な役割は謎として残されていた。我々は、TGF-β/activin刺激による時計リセットにDec1が必須であることを明らかにすると共に、Dec1の誘導にはType IのTGF-β受容体キナーゼ(ALK5: activin receptor-like kinase)による転写因子SMAD3のリン酸化を介した活性化と、それに続くSMAD3-SMAD4のDec1遺伝子上流への結合が重要であることを示した(図2)。このようにして、末梢時計の位相リセットにおける細胞内情報伝達の流れを分子レベルで解明することに初めて成功した。さらに生体での検証を目的としてマウス腹腔内にTGF-βを投与したところ、腎臓や副腎などの末梢時計の位相シフトが観察された。しかし、この位相制御はDec1遺伝子欠損マウスでは観察されない事から、TGFβ-ALK5-SMAD3/4- DEC1という位相制御シグナリングが生体において機能していることを明らかにした (Nat. Cell Biol. 2008)。
記憶の形成や固定化の効率は、一日の時間帯によって大きく異なることが知られている。しかし、これが体内時計による直接的な制御なのか、あるいは活動量などの日内変動に影響された間接的な効果であるのか不明である。もし記憶の形成効率が体内時計によって制御されているとしても、その分子メカニズムは謎に包まれている。我々は、記憶の形成・固定化に時刻依存的制御をもたらす候補因子SCOP (SCN circadian oscillatory protein) に着目し、この分子を軸に、記憶と生物時計という2つの脳機能の分子連関を解析している。SCOPはもともと時計中枢であるSCNにおいて、mRNA量と蛋白質量がサーカディアンリズムを示す分子として清水貴美子らが発見した (FEBS Lett. 1999)。我々はその後、膜ラフトにおいてSCOP がグアニンヌクレオチド遊離型K-Rasと結合して安定化し、K-RasへのGTP結合を阻害することによりRaf/MEK/ERK 経路を負に制御することを明らかにした (J. Biol. Chem. 2003)。清水はその後、海馬に発現するSCOPがカルシウム依存性プロテアーゼCalpainにより分解され、K-Ras/ERK経路を介してCRE依存性の転写を促進することを見出した。前脳特異的SCOP過剰発現マウスをもちいて記憶形成への影響を調べた結果、新奇物体認識テストにおいて長期記憶に異常が見られ、SCOPが海馬依存性の長期記憶形成において重要な役割をしていることを明らかにした (図3;Cell 2007)。以上のようにSCOPは、長期記憶形成と概日時計システムの両方に関与しているので、この二つの脳機能を結びつける「鍵分子」である可能性が高い。このような観点から、Scop欠損マウスや脳の領域特異的にSCOPを過剰発現するトランスジェニックマウスを用いた解析を進めている。
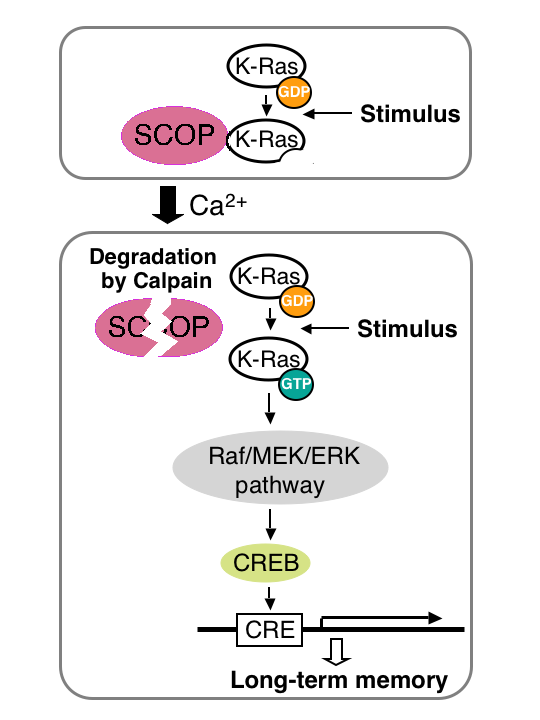 図3.SCOPによる長期記憶形成の制御
[清水貴美子 (2007) 実験医学, Vol. 25, No.14, pp.2181-2184より改変]
図3.SCOPによる長期記憶形成の制御
[清水貴美子 (2007) 実験医学, Vol. 25, No.14, pp.2181-2184より改変]我々はこれまでに、ロドプシン共役G蛋白質トランスデューシン (Gt) の特徴的な脂質修飾を同定し、これが視覚の光シグナリングに必須であることを明らかにした (Nature 1990; Nature 1992など)。これらの脂質修飾がG蛋白質シグナリングにどのように寄与しているかを分子レベルで理解するため、そのγサブユニット (Gtγ) に結合しているファルネシル基の光親和標識化合物を化学合成し、これをGtγに酵素的に転移してファルネシル基が相互作用する分子(群)の同定を試みた。その結果、G蛋白質の活性化と不活性化の状態によって、ファルネシル基が相互作用する標的分子や部位はダイナミックに変化することがわかり、ファルネシル基はきわめて動的な機能制御因子として機能すると考えられた (Biochemistry 2004; Biochemistry 2008)。一方、Gtγがファルネシル化されているのに対し、他のG蛋白質γサブユニットの多くにはゲラニルゲラニル基(より鎖長の長いイソプレノイド)が結合しており、このイソプレノイド選択には何らかの生理的な意味があるのではないかと考えた。これを調べるため、Gtγのファルネシル化を導くアミノ酸配列(ファルネシル化シグナル)をゲラニルゲラニル化シグナルに改変 (Ser74Leu) したノックインマウスを作製した。野生型マウスの桿体視細胞においては、光照射と共にGtβγが外節から内節に移動し、シグナル分子の減少によって光シグナル伝達の効率が低下する(いわゆる明順応)。しかし、Ser74Leu変異マウスの桿体視細胞においては、Gtγの疎水性の増強によってGtβγが外節円板膜から遊離できず、その結果、内節へ移動しにくくなるために明順応が阻害されることがわかった(図4)。Gtγが選択的にファルネシル化されることによりGtはダイナミックに細胞内を移動できるので、ファルネシル化は視細胞の光感度調節(順応)に重要な役割を果たしていることがわかった(Neuron 2005)。G蛋白質のイソプレニル化の生理的意義をより深く理解するために現在、イソプレニル化されない「非修飾型」Gtγを発現するノックインマウスを作製し、桿体視細胞におけるG蛋白質イソプレニル化の生理的意義の徹底的な理解をめざし、個体レベルでの検証を試みている。
脊椎動物の網膜には桿体と錐体という2種類の視細胞が存在し、桿体は高い光感度、錐体は光応答の素早いON/OFF、という異なる光応答特性を示す。我々はこれまで両細胞の光受容分子を単離して性状を詳しく比較し、両者の光応答特性の違いを決定している分子機構を精査してきた(PNAS 1992など)。この研究の中で我々は、錐体の光受容体キナーゼ(GRK7)の分子活性が桿体キナーゼGRK1より数十倍も高いことを見出した(J. Neurochem. 2006)。この違いが両細胞の光応答特性を規定する可能性を検証するため、現在、2種類のGRK遺伝子のトランスジェニックゼブラフィッシュを作製し、単一細胞レベルでの電気生理学的解析と個体レベルでの視覚行動の解析を行っている。
 図4.Gtγのイソプレノイド置換による光応答の生理的変化
[深田吉孝 (2005) 東京大学理学部ニュースVol.37, No.3, p.10より改変]
図4.Gtγのイソプレノイド置換による光応答の生理的変化
[深田吉孝 (2005) 東京大学理学部ニュースVol.37, No.3, p.10より改変]脊椎動物は網膜だけでなく、松果体などの脳組織においても光感受性を示す。我々はこれまでに脳内光受容体の分子実体に焦点を絞って研究を進め、視細胞以外に発現するオプシン型光受容体として世界に先駆けてピノプシンを発見し (Nature 1994)、続いて松果体や脳深部、さらには視細胞以外の網膜ニューロンに発現する種々のオプシン型分子を同定した(例えばJ. Neurosci. 2000; J. Neurochem. 2008など)。しかし、これらの「非視覚型」オプシンを発現するニューロン群がどのような生理現象に関与するのか、その多くは謎に包まれている。小島らは現在、これらのニューロンを選択的かつコンディショナルに破壊することが可能なトランスジェニックゼブラフィッシュを樹立し、非視覚型オプシン発現ニューロン群の個体レベルでの解析を進めている。
一方、脳内光受容組織として研究の進んでいるニワトリ松果体は光感受性の内分泌器官であり、メラトニン分泌量は光刺激で抑制されるが、同時に、内在する概日時計によってもメラトニン分泌量は制御されて夜に上昇する。我々は、ニワトリ松果体のメラトニンリズムを制御する概日時計の光位相シフトにGq型G蛋白質であるG11が関与することを明らかにした(J. Neurosci. 2002)。最近、この光位相シフト経路に関わる光受容分子の有力候補として、2種類のメラノプシン遺伝子をニワトリ松果体において同定し、さらに両遺伝子が青色感受性の光受容分子をコードすることを示した(FEBS Lett. 2007)。現在、組換え蛋白質の再構成系を用いて、メラノプシンがG11経路を光活性化する可能性を調べている。
さて、松果体の光受容ニューロンと網膜の視細胞は、形態学的・進化学的・発生学的に多くの点において類似性を示す一方、両者の生理機能は大きく異なり、網膜視細胞が主として視覚を司り、松果体ニューロンは概日リズム形成と内分泌を担う(Photochem. Photobiol. 2007)。これら2種類の光受容ニューロンのうち、松果体の特異性の獲得や維持に寄与する遺伝子群や転写調節機構はほとんど知られていない状況にあった。我々は、ゼブラフィッシュ松果体に特異的に発現する光受容分子エクソロドプシンを同定し(Mol. Brain Res. 1999)、そのexorh遺伝子のプロモータ解析から、松果体特異的な遺伝子発現を担うシス配列PIPEを初めて同定した (PNAS 2002)。この成果をさらに発展させるため、小島大輔は (1) in vitroにおけるone hybridスクリーニングと (2) in vivoの変異個体スクリーニングを行ない、これらの相互補完的な解析からPIPEに結合する転写因子の同定を試みている(Photochem. Photobiol. 2008)。これとは別のアプローチとして我々は、松果体細胞と視細胞をそれぞれ特異的にGFPでラベルしたトランスジェニック個体を用いて、松果体細胞と視細胞にそれぞれ特異的な遺伝子群のプロファイリングを行っている。これらの網羅的探索法により数種類の松果体特異的な転写因子をすでに同定しており、現在、これらの生理機能を解析すると共に、転写因子間の物理的・遺伝学的な相互作用を検討し、松果体光受容ニューロンの特異性を規定する分子ネットワークの徹底解明を試みている(図5)。
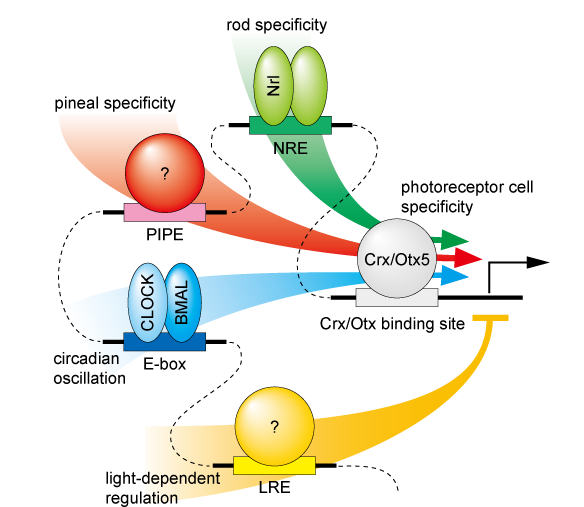 図5.松果体と網膜の光受容細胞における遺伝子発現制御のシスエレメントネットワーク
[真野弘明・深田吉孝 (2007) Photochem. Photobiol.]
図5.松果体と網膜の光受容細胞における遺伝子発現制御のシスエレメントネットワーク
[真野弘明・深田吉孝 (2007) Photochem. Photobiol.]